
ν}ΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
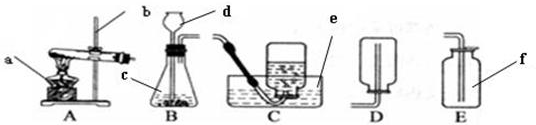
| MnO2 |
| MnO2 |
| MnO2 |
| Γς |
| MnO2 |
| Γς |
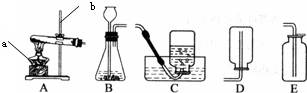 ¨çρû “≥Θ”Οœ¬Ν–―b÷Ο¹μ÷Τ»Γ―θöβΘΚ
¨çρû “≥Θ”Οœ¬Ν–―b÷Ο¹μ÷Τ»Γ―θöβΘΚ| Φ”üα |
| Φ”üα |
| Εΰ―θΜ·εi |
| Εΰ―θΜ·εi |
| ¨çρûΨéΧ• | 1 | 2 |
| Ζ¥ëΣΈο | 5%κp―θΥ° | 5%κp―θΥ° |
| ¥ΏΜ·³© | 1gΦt¥uΖέΡ© | 1gΕΰ―θΜ·εi |
| ïrιg | 165Οκ | 46Οκ |
ΑΌΕ»÷¬–≈ - ΨöΝïÉ‘Ν–±μ - ‘΅ν}Ν–±μ
Κΰ±± ΓΜΞ¬™(li®Δn)ΨW(w®Θng)Ώ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσΤΫ≈_ | ΨW(w®Θng)…œ”–ΚΠ–≈œΔ≈eàσ¨ΘÖ^(q®±) | κä–≈‘pρ_≈eàσ¨ΘÖ^(q®±) | …φöv ΖΧ™üo÷ςΝx”–ΚΠ–≈œΔ≈eàσ¨ΘÖ^(q®±) | …φΤσ«÷ôύ≈eàσ¨ΘÖ^(q®±)
Ώ`Ζ®ΚΆ≤ΜΝΦ–≈œΔ≈eàσκä‘£ΘΚ027-86699610 ≈eàσύ]œδΘΚ58377363@163.com